Содержание
Основные мышцы работающие при плавании
Мышцы пловца выполняют главным образом функции передвижения или стабилизации тела. Обе эти функции необходимы для правильной техники плавания и эффективного перемещения в воде. Ярким примером мышцы, предназначенной для передвижения, служит широчайшая мышца спины, приводящая в движение руку в фазе гребка во всех спортивных стилях плавания. Деятельность стабилизирующих механизмов хорошо иллюстрирует постоянная активность мышц живота.
Пловцу необходимо постоянно прилагать усилия для удерживания тела на поверхности воды. Без поддержания баланса невозможно соблюдение правильной техники, ведь в плавании очень важно управлять своим телом как единым целым. Работа рук и ног должна осуществляться в связке и дополнять друг друга, чтобы не создавалось помех для продвижения вперед.
Уникальной особенностью плавания является то, что пловцы вынуждены сами создавать себе опору при движении, ведь в отличии от наземных видов спорта, пловец не имеет твердой опоры, его окружает жидкая среда. Поэтому ключевым фактором в успешном грамотном плавании служит крепкое туловище, которое одновременно является связующим звеном для согласованных движений рук и ног, и прочной базой, от которой они должны отталкиваться.
Поэтому ключевым фактором в успешном грамотном плавании служит крепкое туловище, которое одновременно является связующим звеном для согласованных движений рук и ног, и прочной базой, от которой они должны отталкиваться.
В ниже приведенной таблице перечислены основные мышцы, задействованные в плавании.
Основные мышцы, отвечающие за движение рук | Основные мышцы, выполняющие стабилизирующие, координирующие и связующие движения рук и ног функции | Основные мышцы, отвечающие за движение ног |
Большая грудная мышца, широчайшая спины, мышцы предплечья, бицепс, плечевая мышца, трицепс, дельтовидная мышца, вращающая манжета плеча (надостная, подостная, малая круглая и подлопаточная мышцы) | Мышцы стабилизирующие положение лопатки (малая грудная, ромбовидные, трапецеевидная, пережняя зубчатая), мышцы стабилизирующие туловище (поперечная живота, прямая живота, косые живота, параспинальные мышцы, мышцы выпрямляющие позвоночник) | Подвздошно-поясничная, четырехглавая бедра, большая и средняя ягодичные, задние мышцы бедра (двуглавая бедра, полусухожильная, полуперепончатая), икроножная, камбаловидная, в брассе кроме перечисленных важное значение имеет группа приводящих мышц на внутренней поверхности бедра |
Понимая, какие именно мышцы задействованы при плавании и какой вклад они вносят в движение, вы сможете сознательно работать над ними и, в конечном итоге, улучшить свою технику и результаты.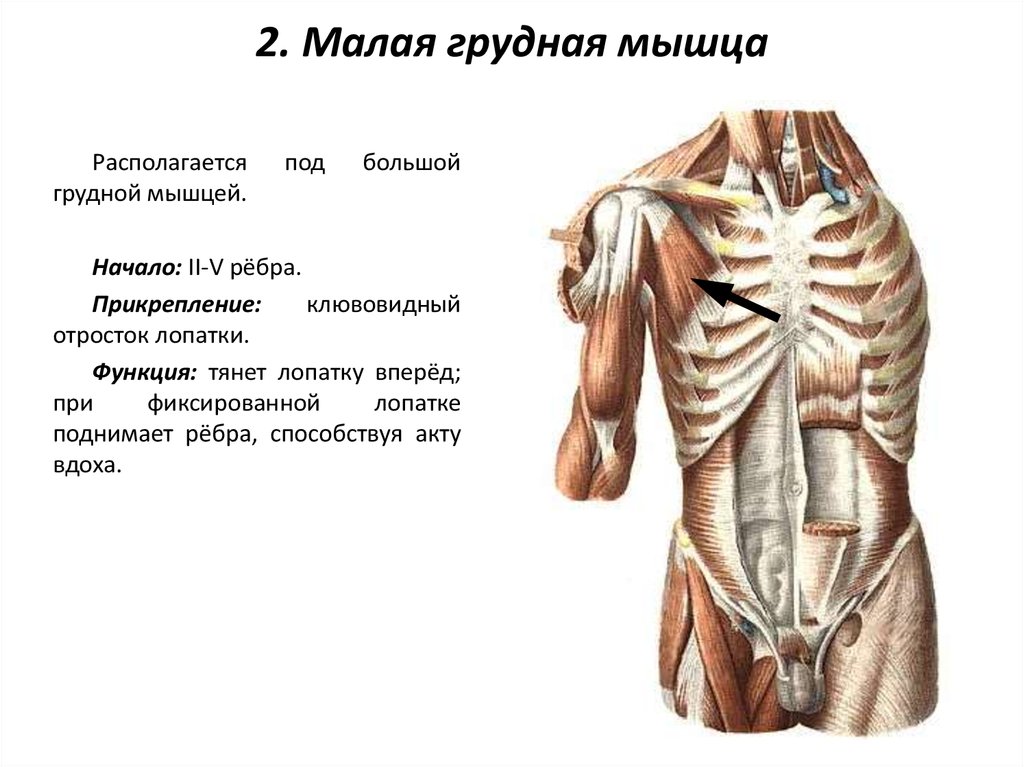
Мышцы туловища и плечевого пояса
Огромный вклад в плавание вносит широчайшая мышца спины, в которой генерируется значительная доля усилий для движения руки (гребка) в подводном положении. Это усилие передается мышцам плечевого пояса и рук.
Трапециевидная и ромбовидная мышцы спины отвечают за движение лопаток, а большая круглая мышца распрямляет плечи.
Вытянутое положение тела при плавание обеспечивает мышца выпрямляющая позвоночник, она отвечает за разгибание позвоночника и за наклон туловища в сторону. Параспинальные мышцы осуществляют поддержку и вращение позвоночника.
Очень важны для пловца мышцы живота. Они осуществляют связь между верхней и нижней частями тела, наклоняют корпус вперед и в стороны, осуществляют повороты и вращение туловища, волнообразные движения в баттерфляе и брасе, стабилизируют положение туловища в воде. Прямая мышца ответственна за наклон туловища вперед и подтягивание таза к груди. Боковые мышцы живота (косые и поперечная) поворачивают корпус по продольной оси, помогают наклону вперед и поддержанию позы.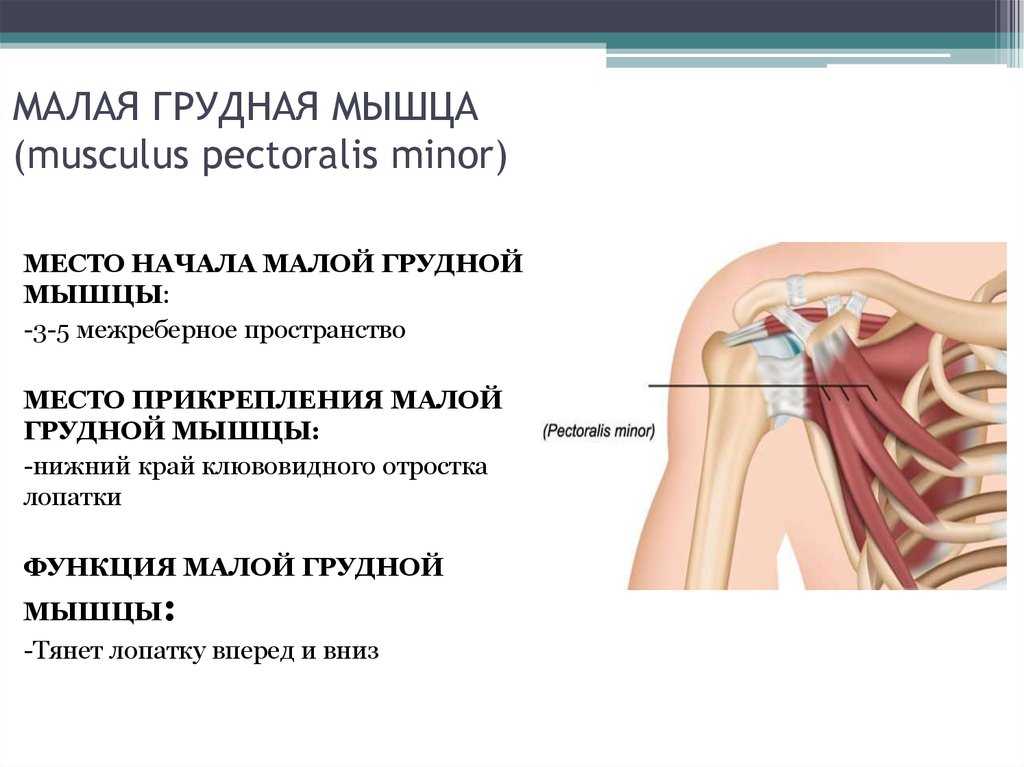
Второй из главных мышц (первая – широчайшая спины), приводящих руку пловца в движение в подводной фазе гребка, является большая грудная мышца. Сокращаясь, большая грудная мышца притягивает к себе плечевую кость, за счет чего совершаются движения в плечевом суставе.
Передняя зубчатая мышца и малая грудная мышца отвечают за движение лопатки и участвуют в стабилизации ее положения. Вращающая манжета плеча (надостная, подостная, малая круглая и подлопаточная мышцы) защищает и стабилизирует плечевой сустав, обеспечивает его вращательные движения.
Дельтовидная мышца отвечает за позиционирование плечевого сустава, эта мышца особенно активна в фазе проноса.
Мышцы рук
С помощью рук усилия большой грудной и широчайшей мышцы спины преобразуются в передвижение пловца в воде.
Трицепс (трехглавая мышца плеча) разгибает руку в локтевом суставе. Локтевая мышца помогает трицепсу и стабилизирует локтевой сустав. За сгибание руки в локтевом суставе ответственны бицепс (двуглавая мышца плеча) и плечевая мышцы.
Мышцы предплечья отвечают за движение кисти и пальцев, сгибание запястья.
Мышцы ног
Группа передних мышц бедра и таза ответственны за движения в тазобедренном и коленном суставе. Подвздошно-поясничная мышца сгибает ногу в тазобедренном суставе. Четырехглавая мышца бедра – самая крупная мышца в теле человека – разгибает ногу в коленном суставе и помогает сгибать ногу в тазобедренном суставе. Напрягатель широкой фасции бедра и портняжная мышца ответственны за сгибание и отведение ноги в тазобедренном суставе, вращение ноги.
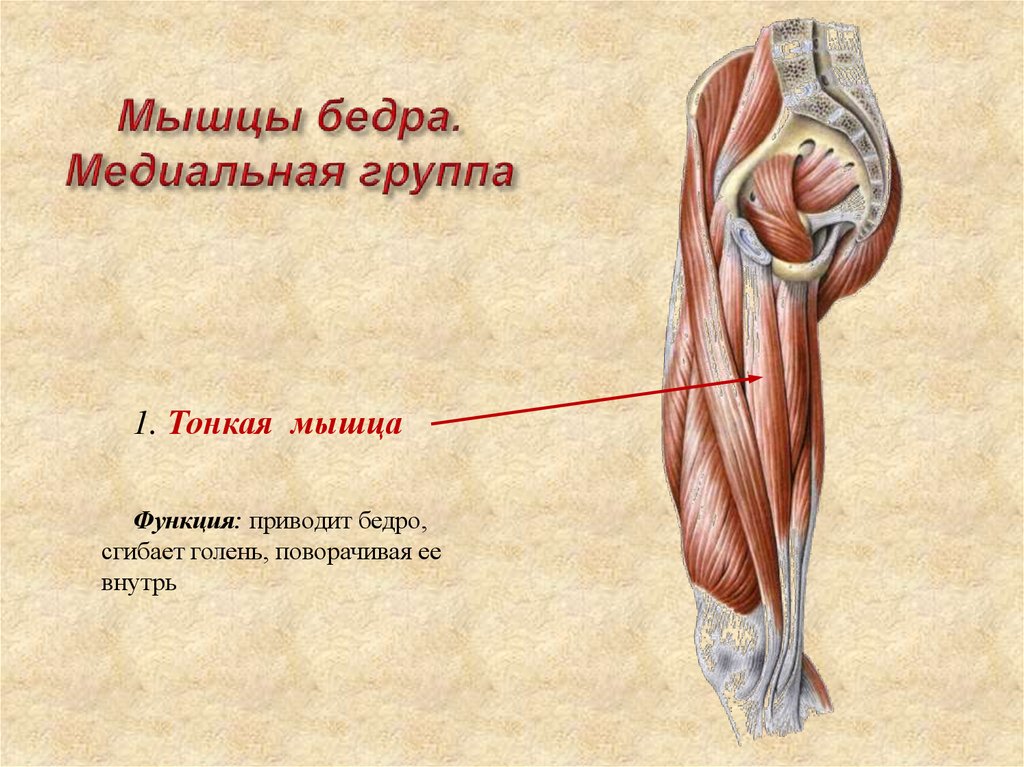
Функция группы приводящих мышц заключается в приведении ноги в тазобедренном суставе. Приводить ногу помогают гребенчатая и тонкая мышцы, которые также содействуют сгибанию в тазобедренном (гребенчатая) и коленном (тонкая) суставах.
Ягодичные мышцы разгибают ноги в тазобедренном суставе, отвечают за отведение и вращение ноги.
Группа задних мышц бедра (двуглавая мышца бедра, полуперепончатая, полусухожильная) отвечает за разгибание ноги в тазобедренном и сгибание в коленном суставе.
Мышцы голени (икроножная, камбаловидная, большеберцовые и малоберцовые мышцы) управляют движениями в голеностопном суставе.
Посмотреть по теме:
Фильмы о специальной физической подготовке пловца (упражнения, тренажеры, инвентарь)
Источник: http://plavaem.info/glavnye_myshzy_plovza.php
Роль лоскута большой грудной мышцы в спасительной тотальной ларингэктомии | Ларингология | JAMA Отоларингология – Хирургия головы и шеи
Абстрактный
Цель
Оценить полезность лоскута большой грудной мышцы (PMMF) у пациентов, перенесших тотальную ларингэктомию.
Дизайн
Ретроспективный когортный анализ.
Настройка
Третичный онкологический центр.
Пациенты
В исследование включен 461 пациент, перенесший ларингэктомию. Восемьдесят из них подверглись спасительной операции с первичным закрытием глотки.
Вмешательства
Из 80 пациентов 69 (86 %) подверглись только первичному закрытию глотки, а 11 (14 %) — PMMF, который использовался для укрепления линии глоточного шва.
Показатель основного результата
Двести тридцать шесть переменных были зарегистрированы для каждого пациента. Были измерены осложнения, связанные с закрытием глотки.
Результаты
Шестьдесят четыре процента пациентов, перенесших PMMF, также прошли химиолучевую терапию в качестве начального радикального лечения по сравнению с 25 % в группе без PMMF ( P = 0,03). При многомерном анализе химиолучевая терапия была единственным независимым предиктором образования кожно-глоточных свищей (относительный риск 1,82; P = 0,02). Тем не менее, частота фарингокожных свищей была одинаковой в группах PMMF (27%) и без PMMF (24%). Кроме того, в обеих группах были зарегистрированы сходные продолжительность кормления через зонд, количество дней до кормления через рот и период госпитализации.
Заключение
PMMF следует разумно использовать в качестве вспомогательного хирургического средства у пациентов с высоким риском с целью сведения к минимуму риска развития кожно-глоточных свищей.
В результате разработки стратегий органосохранения для пациентов с распространенным раком гортани начальная тотальная ларингэктомия (TLR) в настоящее время выполняется в основном в случаях, связанных с первичными опухолями с обширной инвазией хряща или экстраларингеальным поражением мягких тканей. 1 Пациенты с плохой функцией гортани (несостоятельность гортани) на момент постановки диагноза также могут получить пользу от первичного TLR, поскольку функциональное восстановление после консервативного лечения маловероятно. В случае персистенции или рецидива опухоли после первичного лучевого или химиолучевого лечения единственным оставшимся вариантом лечения является хирургическое вмешательство в виде спасительной частичной ларингэктомии или TLR. 2 ,3 Тип предшествующего лечения, размер опухоли и клиническое состояние пациента обычно определяют тип необходимой хирургической процедуры. 4 Несмотря на воспроизводимость хирургической техники ТЛР, эта процедура по-прежнему сопряжена с высоким риском формирования послеоперационных глоточно-кожных свищей (ЗКФ), особенно если она выполняется менее чем через 1 год после первичного лучевого лечения. 5 Традиционно клинические исследования документально подтверждают 10–20% случаев ПКФ после TLR. 6 -8 Эти исследования в основном основаны на первичном TLR. За последнее десятилетие несколько исследований продемонстрировали улучшение результатов и более высокую степень сохранения гортани после химиолучевой терапии по сравнению с только лучевой терапией при распространенном раке гортани. 9 ,10 Благодаря этому уровню доказательности I химиолучевая терапия стала стандартом лечения подходящих пациентов. 11 ,12 Однако комбинация химиотерапии и лучевой терапии может привести к более высокому риску образования ПЗК после спасительного TLR.
4 Несмотря на воспроизводимость хирургической техники ТЛР, эта процедура по-прежнему сопряжена с высоким риском формирования послеоперационных глоточно-кожных свищей (ЗКФ), особенно если она выполняется менее чем через 1 год после первичного лучевого лечения. 5 Традиционно клинические исследования документально подтверждают 10–20% случаев ПКФ после TLR. 6 -8 Эти исследования в основном основаны на первичном TLR. За последнее десятилетие несколько исследований продемонстрировали улучшение результатов и более высокую степень сохранения гортани после химиолучевой терапии по сравнению с только лучевой терапией при распространенном раке гортани. 9 ,10 Благодаря этому уровню доказательности I химиолучевая терапия стала стандартом лечения подходящих пациентов. 11 ,12 Однако комбинация химиотерапии и лучевой терапии может привести к более высокому риску образования ПЗК после спасительного TLR. 13 В результате в этой популяции было зарегистрировано увеличение заболеваемости и тяжести PCF. 4 ,14
13 В результате в этой популяции было зарегистрировано увеличение заболеваемости и тяжести PCF. 4 ,14
В недавнем метаанализе 26 исследований Paydarfar и Birkmeyer 13 выявил несколько существенных факторов риска образования свищей. Из 10 проанализированных переменных 4 были в значительной степени связаны с ПЗК, включая послеоперационный уровень гемоглобина менее 12,5 г/дл (для преобразования в граммы на литр умножьте на 10), предшествующую трахеотомию, предоперационную лучевую терапию и предоперационную лучевую терапию и одновременную рассечение шеи. Доза лучевой терапии, время от лучевой терапии до операции, сопутствующие заболевания, локализация опухоли, стадия опухоли и одновременная диссекция шеи не были статистически значимыми. Чтобы справиться с этой серьезной послеоперационной заболеваемостью, несколько авторов выступают за рутинное использование лоскута большой грудной мышцы (PMMF) [9].0041 15 ,16 лоскут воротника грудино-ключично-сосцевидной мышцы, 17 или свободный лоскут 18 для спасения TLR с целью укрепления линии первичного глоточного шва васкуляризированной тканью. Цель нашего исследования заключалась в том, чтобы сообщить об исходах у пациентов, перенесших TLR спасения, у которых использовалась PMMF, с целью минимизации риска образования PCF.
Цель нашего исследования заключалась в том, чтобы сообщить об исходах у пациентов, перенесших TLR спасения, у которых использовалась PMMF, с целью минимизации риска образования PCF.
Методы
Это ретроспективное исследование случай-контроль было основано на обзоре больничных и амбулаторных клинических карт 461 пациента, перенесших частичную ларингэктомию или TLR по поводу рака гортани в Мемориальном онкологическом центре Слоана-Кеттеринга, Нью-Йорк, Нью-Йорк, между 1991 и 2006. В это исследование были включены только пациенты, у которых первичная лучевая или химиолучевая терапия оказалась неэффективной и которым потребовалась спасительная TLR. Пациенты, перенесшие частичную ларингэктомию, фарингэктомию или резекцию основания языка, а также пациенты, нуждающиеся в реконструкции глотки лоскутом, не были включены в эту когорту. В наше исследование было включено 80 пациентов, 69 из которых (86%) подверглись первичному закрытию неоглотки после удаления опухоли без усиления ПММП (группа без ПММП). Остальным 11 пациентам (14%) было выполнено первичное закрытие глотки, которое затем было усилено ПМФМ (группа ПММФ). Клинические и демографические характеристики пациентов были зарегистрированы и проанализированы ретроспективно. Послеоперационные осложнения считались «ранними», если они возникли в течение 30 дней после операции. Осложнения, связанные с закрытием глотки, измеряли путем регистрации следующих параметров: ЗЧФ, местные раневые осложнения, повторная операция по реконструкции глотки, продолжительность назогастрального кормления, дни до полного перорального питания и продолжительность госпитализации. Всего для каждого пациента было записано 236 переменных. Сопутствующую патологию пациентов регистрировали с помощью индекса коморбидности Charlson. 19 Клинические, демографические и опухолевые параметры были проанализированы с использованием непараметрических качественных и количественных тестов. Точный критерий Фишера (StatCalc 2.0, Университет Луизианы, Лафайет) использовался, когда количество событий было меньше 10.
Остальным 11 пациентам (14%) было выполнено первичное закрытие глотки, которое затем было усилено ПМФМ (группа ПММФ). Клинические и демографические характеристики пациентов были зарегистрированы и проанализированы ретроспективно. Послеоперационные осложнения считались «ранними», если они возникли в течение 30 дней после операции. Осложнения, связанные с закрытием глотки, измеряли путем регистрации следующих параметров: ЗЧФ, местные раневые осложнения, повторная операция по реконструкции глотки, продолжительность назогастрального кормления, дни до полного перорального питания и продолжительность госпитализации. Всего для каждого пациента было записано 236 переменных. Сопутствующую патологию пациентов регистрировали с помощью индекса коморбидности Charlson. 19 Клинические, демографические и опухолевые параметры были проанализированы с использованием непараметрических качественных и количественных тестов. Точный критерий Фишера (StatCalc 2.0, Университет Луизианы, Лафайет) использовался, когда количество событий было меньше 10. χ 2 Тесты (отношение правдоподобия) и модель пропорциональных рисков Кокса (JMP; SAS Institute Inc, Cary, Северная Каролина) использовались для сравнительного анализа. Исследование было одобрено институциональным наблюдательным советом.
χ 2 Тесты (отношение правдоподобия) и модель пропорциональных рисков Кокса (JMP; SAS Institute Inc, Cary, Северная Каролина) использовались для сравнительного анализа. Исследование было одобрено институциональным наблюдательным советом.
Результаты
Предикторы осложнений, связанные с пациентом и операцией, были изучены в случаях с PMMF или без него. В таблице 1 представлены основные клинико-демографические характеристики каждой группы. Следующие параметры были одинаковыми в обеих группах: возраст, пол, индекс сопутствующей патологии, уровень гемоглобина, уровень альбумина, индекс массы тела, доза облучения, маргинальный статус, инвазия хряща, стадия TNM до спасительной операции, предшествующая трахеостомия, метод ушивания глотки и вовлечение грушевидного синуса. У пациентов, перенесших закрытие глотки с помощью PMMF, была более высокая доля надгортанных опухолей (45% против 1,5%; 9).0031 P < 0,001) и частота первичной химиолучевой терапии в 2,56 раза выше (64% против 25%) по сравнению с пациентами без усиления PMMF, соответственно ( P = 0,03).
Анализ переменных, связанных с успехом закрытия глотки, показал, что в целом у 24% (16 из 69) пациентов в группе без PMMF развилась ЗЧФ по сравнению с 27% (3 из 11) пациентов в группе без PMMF. группа PMMF ( P = 0,70). Точно так же пациенты, перенесшие только первичное закрытие, и пациенты с реконструкцией PMMF имели одинаковую продолжительность кормления через назогастральный зонд (среднее [SD], 15 [16] дней против 16 [4] дней), дней до полного перорального питания (среднее [SD], 10 [14] дней против 12 [8] дней) и продолжительность госпитализации (среднее [SD], 16 [10] дней против 17 [4] дней). Частота раневых осложнений (гематомы, подкожная эмфизема, местная инфекция) также была одинаковой в обеих группах. Ни у одного из пациентов не было свища, сохраняющегося более 30 дней после операции. В таблице 2 приведены осложнения и течение послеоперационного периода в обеих группах.
Восьми из 16 пациентов (50%) с ЗКП, которые не получали ПМФМ, потребовалась повторная хирургическая процедура для закрытия фистулы.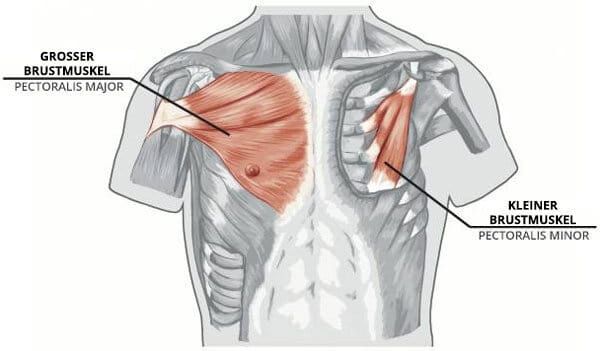 С другой стороны, ни один из пациентов в группе PMMF, у которых развилась ЗЧФ, не нуждался во второй операции ( P < 001). Для выявления факторов, связанных с протечками, требующими повторной операции в группе без PMMF, мы дополнительно проанализировали следующие параметры: возраст, пол, оперирующий хирург, индекс сопутствующей патологии, злоупотребление алкоголем и никотином в анамнезе, уровень альбумина, уровень гемоглобина, индекс массы тела. , первичная локализация опухоли, количество пораженных подзон, предшествующая химиотерапия, стадия опухоли, доза облучения, инвазия в хрящ, инвазия в щитовидную железу, вовлечение грушевидного синуса, вовлечение боковой стенки глотки, состояние краев, экстракапсулярное распространение, использование первичной трахеопищеводной пункции, тип закрытия, и возникновение других осложнений. Ни один из этих факторов не был связан с серьезными утечками, требующими хирургического вмешательства.
С другой стороны, ни один из пациентов в группе PMMF, у которых развилась ЗЧФ, не нуждался во второй операции ( P < 001). Для выявления факторов, связанных с протечками, требующими повторной операции в группе без PMMF, мы дополнительно проанализировали следующие параметры: возраст, пол, оперирующий хирург, индекс сопутствующей патологии, злоупотребление алкоголем и никотином в анамнезе, уровень альбумина, уровень гемоглобина, индекс массы тела. , первичная локализация опухоли, количество пораженных подзон, предшествующая химиотерапия, стадия опухоли, доза облучения, инвазия в хрящ, инвазия в щитовидную железу, вовлечение грушевидного синуса, вовлечение боковой стенки глотки, состояние краев, экстракапсулярное распространение, использование первичной трахеопищеводной пункции, тип закрытия, и возникновение других осложнений. Ни один из этих факторов не был связан с серьезными утечками, требующими хирургического вмешательства.
Наконец, для выявления факторов, связанных с формированием ЗЧЯ, был проведен многофакторный анализ всей исследуемой популяции (80 пациентов с ПМФМ или без нее). Этот анализ показал, что единственным значимым независимым фактором риска развития ПЗК было предшествующее химиолучевое лечение ( P = 02). Дальнейший анализ показал, что риск образования ПЗК после химиолучевой терапии составил 39% по сравнению с 21% после только лучевой терапии (относительный риск 1,83).
Этот анализ показал, что единственным значимым независимым фактором риска развития ПЗК было предшествующее химиолучевое лечение ( P = 02). Дальнейший анализ показал, что риск образования ПЗК после химиолучевой терапии составил 39% по сравнению с 21% после только лучевой терапии (относительный риск 1,83).
Поскольку многие пациенты, перенесшие ларингэктомию, нуждаются в относительно длительной госпитализации из-за сопутствующих заболеваний, мы рассматривали продолжительность пребывания в больнице более 30 дней как длительный период госпитализации. Ни один из пациентов с PMMF не находился в больнице более 30 дней, в то время как 7 пациентов в группе без PMMF были госпитализированы более 30 дней. Если Pa и Pb представляют собой вероятность длительной госпитализации в группе с PMMF и без PMMF, соответственно, то число, необходимое для лечения (рассчитывается как 1/[ p b – p a ]) составляет 11 пациентов.
Комментарий
Разработка органосохраняющих программ химиотерапии с лучевой терапией произвела революцию в лечении пациентов с поздними стадиями рака гортани.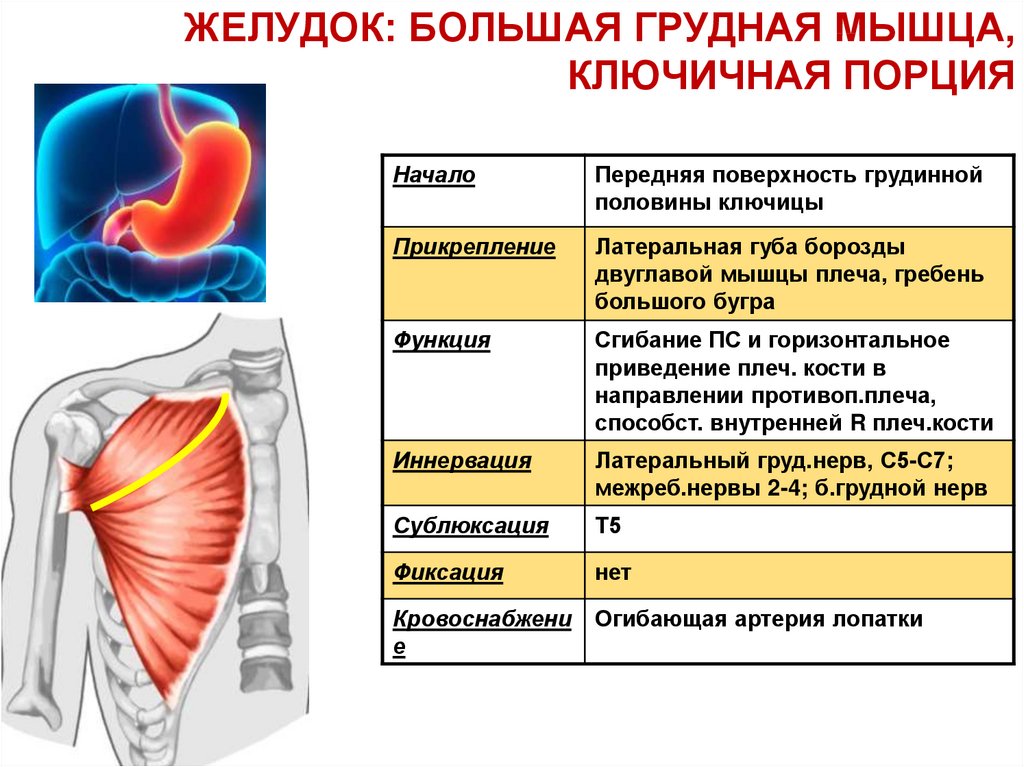 10 ,14 ,20 Хотя было обнаружено, что лучевая терапия с одновременным введением цисплатина превосходит только лучевую терапию для сохранения гортани и местного контроля, 10 ассоциировалось с 2-кратным увеличением частоты образования ПКФ. 4 ,14 Учитывая увеличение частоты свищей в этой популяции, PMMF был предложен в качестве метода укрепления линии глоточного шва после TLR. Считалось, что объем хорошо васкуляризированной необлученной ткани, примыкающей к закрытию глотки, может снизить частоту местных раневых осложнений.
10 ,14 ,20 Хотя было обнаружено, что лучевая терапия с одновременным введением цисплатина превосходит только лучевую терапию для сохранения гортани и местного контроля, 10 ассоциировалось с 2-кратным увеличением частоты образования ПКФ. 4 ,14 Учитывая увеличение частоты свищей в этой популяции, PMMF был предложен в качестве метода укрепления линии глоточного шва после TLR. Считалось, что объем хорошо васкуляризированной необлученной ткани, примыкающей к закрытию глотки, может снизить частоту местных раневых осложнений.
Основная цель нашего исследования заключалась в том, чтобы выяснить, связано ли использование PMMF с более низкой частотой PCF, меньшим временем до перорального кормления и сокращением времени госпитализации в группе высокого риска. Многомерный анализ был использован для выявления факторов, связанных с повышенным риском образования ПЗК после спасительного TLR. В соответствии с предыдущими отчетами мы показали, что предшествующая химиолучевая терапия была связана с повышением риска образования свищей на 18%.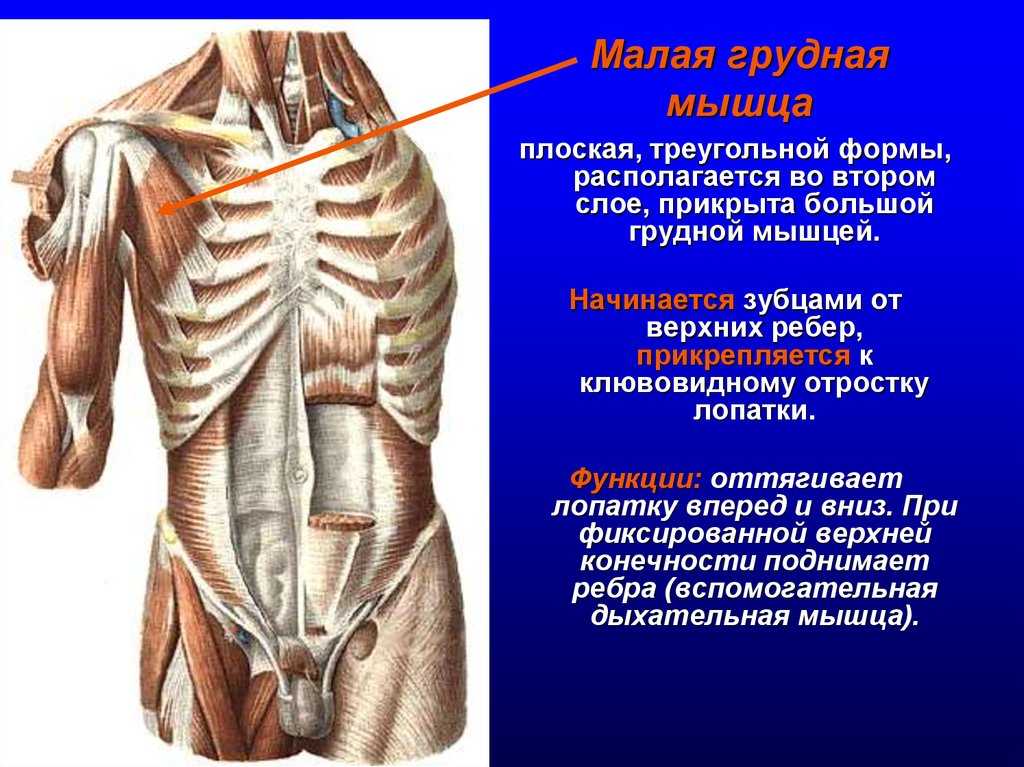 4 ,14 Однако, несмотря на то, что 64% пациентов в группе ПМФМ ранее получали химиолучевую терапию по сравнению с 25% в группе без ПМФМ, мы не обнаружили различий в частоте формирования ПКФ, местных раневых осложнений, дней к пероральному кормлению и пребыванию в стационаре между двумя группами. Поскольку было показано, что сопутствующая диссекция шеи связана с повышенным риском образования ПЗК, следует отметить, что у большинства пациентов в нашем исследовании не было лимфатических узлов.
4 ,14 Однако, несмотря на то, что 64% пациентов в группе ПМФМ ранее получали химиолучевую терапию по сравнению с 25% в группе без ПМФМ, мы не обнаружили различий в частоте формирования ПКФ, местных раневых осложнений, дней к пероральному кормлению и пребыванию в стационаре между двумя группами. Поскольку было показано, что сопутствующая диссекция шеи связана с повышенным риском образования ПЗК, следует отметить, что у большинства пациентов в нашем исследовании не было лимфатических узлов.
Существует большая вариабельность зарегистрированных показателей ЗКФ после ларингэктомии, частота которой колеблется от 2,6% до 66%. 13 Эта изменчивость в значительной степени может быть объяснена различиями в периоде исследования, характеристиках пациентов, опыте хирурга и предшествующем лечении. Наша скорость образования ЗКФ аналогична той, о которой сообщалось в других исследованиях пациентов, перенесших спасительную ТЛР. 4 ,14 ,21 -25
В нескольких исследованиях специально изучалась полезность PMMF для укрепления линии глоточного шва после TLR. Смит и др. 15 сравнили свои результаты с PMMF с результатами исторической когорты, которая была подвергнута хирургическому лечению без грудных лоскутов, и сообщили о значительном снижении скорости развития ПЗК (с 23% до 1%). Они пришли к выводу, что PMMF должна стать стандартной техникой TLR для предотвращения PCF. В их исследовании только 25% пациентов ранее проходили лучевую терапию, а количество пациентов, получивших химиолучевую терапию, не сообщалось. 15 В более поздней статье Righini et al 16 сообщили о своем опыте работы с пациентами, перенесшими спасительную ТЛР (25% из них получили химиолучевую терапию), и сообщили о снижении частоты ПКФ с 50% без PMMF до 23% с лоскутом. Однако это различие не достигло статистической значимости. Аналогичные результаты были описаны Albirmawy 17 для лоскута грудино-ключично-сосцевидной мышцы. Недавно Fung et al. 18 также исследовал рутинное использование свободного радиального предплечья или переднебокового бедренного лоскута для укрепления линии глоточного шва у пациентов, подвергающихся спасительной TLR.
Смит и др. 15 сравнили свои результаты с PMMF с результатами исторической когорты, которая была подвергнута хирургическому лечению без грудных лоскутов, и сообщили о значительном снижении скорости развития ПЗК (с 23% до 1%). Они пришли к выводу, что PMMF должна стать стандартной техникой TLR для предотвращения PCF. В их исследовании только 25% пациентов ранее проходили лучевую терапию, а количество пациентов, получивших химиолучевую терапию, не сообщалось. 15 В более поздней статье Righini et al 16 сообщили о своем опыте работы с пациентами, перенесшими спасительную ТЛР (25% из них получили химиолучевую терапию), и сообщили о снижении частоты ПКФ с 50% без PMMF до 23% с лоскутом. Однако это различие не достигло статистической значимости. Аналогичные результаты были описаны Albirmawy 17 для лоскута грудино-ключично-сосцевидной мышцы. Недавно Fung et al. 18 также исследовал рутинное использование свободного радиального предплечья или переднебокового бедренного лоскута для укрепления линии глоточного шва у пациентов, подвергающихся спасительной TLR. Они сообщили об аналогичной частоте ЗКФ в группе со свободным лоскутом (29).%) и их контрольная группа (30%). Эти исследования и наблюдения в нашем текущем отчете показывают, что риск образования свищей в группе высокого риска у пациентов, нуждающихся в TLR, значительно снижен и подобен риску в группе пациентов, у которых, как считалось, ткани были достаточно здоровыми, а не требуется усиление линии глоточного шва с помощью PMMF.
Они сообщили об аналогичной частоте ЗКФ в группе со свободным лоскутом (29).%) и их контрольная группа (30%). Эти исследования и наблюдения в нашем текущем отчете показывают, что риск образования свищей в группе высокого риска у пациентов, нуждающихся в TLR, значительно снижен и подобен риску в группе пациентов, у которых, как считалось, ткани были достаточно здоровыми, а не требуется усиление линии глоточного шва с помощью PMMF.
Хорошо известно, что продолжительность времени до закрытия ЗКП больше, если ткани были облучены. 26 В нашем исследовании у 16 пациентов, перенесших ушивание глотки без PMMF, развилась ЗЧФ, и 50% из них потребовалось ревизионное хирургическое вмешательство для закрытия фистулы. Для сравнения, ни одному из пациентов в группе PMMF не потребовалась повторная операция. Вполне возможно, что фистула у этих пациентов была более локализованной и ее можно было лечить консервативно. В качестве альтернативы также возможно, что пациенты, получившие PMMF, исчерпали все доступные реконструктивные варианты и, следовательно, должны были лечиться консервативно. Однако, поскольку ни у одного из наших пациентов свищ не развился более чем через 30 дней после TLR, мы пришли к выводу, что PMMF принес здоровую, необлученную васкуляризированную ткань по линии шва, что позволило спонтанно закрыть свищ без необходимости хирургического вмешательства. Таким образом, у пациентов, у которых развилась ЗЧФ, ПМФ, по-видимому, ограничивает тяжесть свища и снижает потребность в ревизионной операции.
Однако, поскольку ни у одного из наших пациентов свищ не развился более чем через 30 дней после TLR, мы пришли к выводу, что PMMF принес здоровую, необлученную васкуляризированную ткань по линии шва, что позволило спонтанно закрыть свищ без необходимости хирургического вмешательства. Таким образом, у пациентов, у которых развилась ЗЧФ, ПМФ, по-видимому, ограничивает тяжесть свища и снижает потребность в ревизионной операции.
Очевидно, существует несколько ограничений, связанных с ретроспективным дизайном нашего исследования. Во-первых, небольшое количество пациентов, включенных в наше исследование, ограничивает нашу способность делать убедительные выводы на основе данных. Во-вторых, несмотря на то, что в нашу базу данных было занесено более 200 позиций, на вопрос о том, какие факторы повлияли на решение хирурга выполнить реконструкцию PMMF, трудно ответить полностью. Одна из гипотез состоит в том, что озабоченность опытного хирурга во время операции потенциальным риском образования свищей является разумным отражением повышенного риска ЗЧФ. Единственными существенными различиями, которые мы обнаружили между двумя группами пациентов, были предшествующее химиолучевое лечение и надгортанное происхождение первичной опухоли. Другие факторы, такие как натяжение линии шва, рыхлость слизистой оболочки глотки и фиброз, трудно поддаются количественной оценке и недоступны для анализа. Эти важные переменные потенциально могут повлиять на частоту осложнений, а также могут повлиять на решение хирурга о том, следует ли использовать PMMF.
Единственными существенными различиями, которые мы обнаружили между двумя группами пациентов, были предшествующее химиолучевое лечение и надгортанное происхождение первичной опухоли. Другие факторы, такие как натяжение линии шва, рыхлость слизистой оболочки глотки и фиброз, трудно поддаются количественной оценке и недоступны для анализа. Эти важные переменные потенциально могут повлиять на частоту осложнений, а также могут повлиять на решение хирурга о том, следует ли использовать PMMF.
В нашем исследовании PMMF чаще применялся у пациентов с надгортанными опухолями. В этой группе опухолей маргинальной зоны возможно, что закрытие остаточной слизистой могло потребовать аппроксимации фарингэктомического дефекта под большим натяжением, чем в других случаях, когда ларингэктомия выполнялась по поводу опухолей голосовой щели. Поэтому вполне вероятно, что субъективные факторы, такие как натяжение линии шва, могли способствовать еще большему риску осложнений в этой группе.
Мы пришли к выводу, что PMMF не следует использовать в качестве рутинной процедуры у пациентов, которым требуется реанимация TLR (у которых общая частота PCF ниже 30%). Ввиду повышенной заболеваемости, времени и стоимости добавления PMMF (васкуляризированной ткани) для укрепления линии глоточного шва, эту процедуру следует использовать с осторожностью у пациентов с предшествующим химиолучевым лечением и у пациентов с плохим нутритивным статусом. Кроме того, следует учитывать размер хирургического дефекта и васкуляризацию тканей по линии глоточного шва. Таким образом, в выбранной популяции пациентов с высоким риском ПЗК PMMF может быть ценным дополнением для снижения риска осложнений, заболеваемости и потенциальной необходимости ревизионной операции.
Ввиду повышенной заболеваемости, времени и стоимости добавления PMMF (васкуляризированной ткани) для укрепления линии глоточного шва, эту процедуру следует использовать с осторожностью у пациентов с предшествующим химиолучевым лечением и у пациентов с плохим нутритивным статусом. Кроме того, следует учитывать размер хирургического дефекта и васкуляризацию тканей по линии глоточного шва. Таким образом, в выбранной популяции пациентов с высоким риском ПЗК PMMF может быть ценным дополнением для снижения риска осложнений, заболеваемости и потенциальной необходимости ревизионной операции.
В заключение следует отметить, что предыдущее химиолучевое лечение является независимым фактором риска образования ПЗК после спасительного TLR. PMMF следует использовать с осторожностью в качестве хирургического дополнения для укрепления линии глоточного шва у пациентов с высоким риском образования ЗКФ.
Адрес для переписки: Зив Гиль, доктор медицинских наук, лаборатория прикладных исследований рака, служба хирургии основания черепа, отделение отоларингологии – хирургии головы и шеи, Тель-Авивский медицинский центр Сураски, ул. Вейцмана, 6, Тель-Авивский университет, 64239Тель-Авив, Израиль ([email protected]).
Вейцмана, 6, Тель-Авивский университет, 64239Тель-Авив, Израиль ([email protected]).
Подано для публикации: 25 ноября 2008 г.; окончательная редакция получена 29 января 2009 г.; принято 10 февраля 2009 г.
Вклад авторов: Доктора Гил и Патель имели полный доступ ко всем данным исследования и несут ответственность за целостность данных и точность анализа данных. Концепция и дизайн исследования : Гил, Краус, Шах и Патель. Сбор данных : Гил, Гупта, Куммер и Патель. Анализ и интерпретация данных : Гил, Кордейро, Краус и Патель. Составление рукописи : Гил, Куммер и Патель. Критический пересмотр рукописи на предмет важного интеллектуального содержания : Гил, Гупта, Кордейро, Краус, Шах и Патель. Статистический анализ : Гил и Патель. Получено финансирование : Гил. Административная, техническая и материальная поддержка : Куммер. Надзор за исследованием : Кордейро, Краус, Шах и Патель.
Раскрытие финансовой информации: Не сообщалось.
Дополнительные материалы: Нэнси Беннет предоставила редакторскую помощь.
использованная литература
1.
Группа по изучению рака гортани Департамента по делам ветеранов. Индукционная химиотерапия в сочетании с лучевой терапией по сравнению с хирургическим вмешательством в сочетании с лучевой терапией у пациентов с распространенным раком гортани. N Engl J Med 1991;324
(24)
1685- 1690PubMedGoogle ScholarCrossref
2.
Краус
DHPfister
Д.Гаррисон
ФУНТ
и другие. Спасательная ларингэктомия при неудачной терапии с сохранением гортани. Энн Отол Ринол Ларингол 1995;104
(12)
936- 941PubMedGoogle Scholar
3.
Holsinger
FCFunk
ЭРобертс
ДБДиаз
ЭМ
Jr Консервационная хирургия гортани по сравнению с тотальной ларингэктомией при лучевой недостаточности при раке гортани. Шея головы 2006;28
(9)
779- 784PubMedGoogle ScholarCrossref
4.
Ганли
IPатель
С.Матсуо
Дж
и другие. Послеоперационные осложнения тотальной ларингэктомии. Рак 2005;103
(10)
2073- 2081PubMedGoogle ScholarCrossref
5.
Засслер
AMESclamado
РМВольф
Хирургия ГТ после органосохраняющей терапии: анализ раневых осложнений. Arch Otolaryngol Head Neck Surg 1995;121
(2)
162- 165PubMedGoogle ScholarCrossref
6.
Роббинс
JPMarks
RMFitz-Хью
Констебль
WC Непосредственные осложнения ларингэктомии после высокодозной предоперационной лучевой терапии.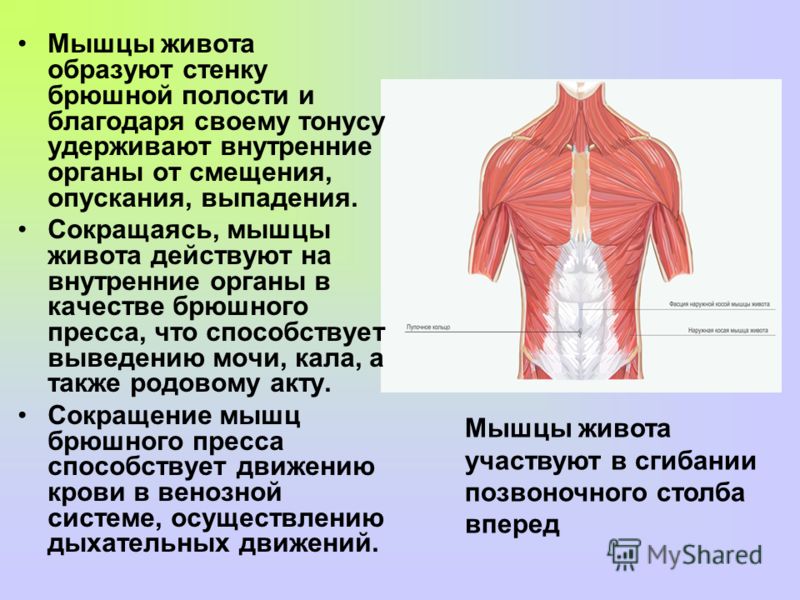 Рак 1972;30
Рак 1972;30
(1)
91- 96PubMedGoogle ScholarCrossref
7.
Каммингс
CWДжонсон
ДжЧунг
CKSagerman
R Осложнения ларингэктомии и расслоения шеи после плановой предоперационной лучевой терапии. Энн Отол Ринол Ларингол 1977;86
(6, часть 1)
745- 750PubMedGoogle Scholar
8.
Вэй
ВИЛам
ХВонг
Джонг
GB Кожно-глоточный свищ, осложняющий тотальную ларингэктомию. Aust N Z J Surg 1980; 50
(4)
366- 369PubMedGoogle ScholarCrossref
9.
Лефевр
Дж.Л.Шевалье
Д.Лубоинский
Киркпатрик
Коллетт
Л.Сахмуд
Кооперативная группа по раку головы и шеи TEORTC, Сохранение гортани при раке грушевидной пазухи: предварительные результаты исследования фазы III Европейской организации по исследованию и лечению рака.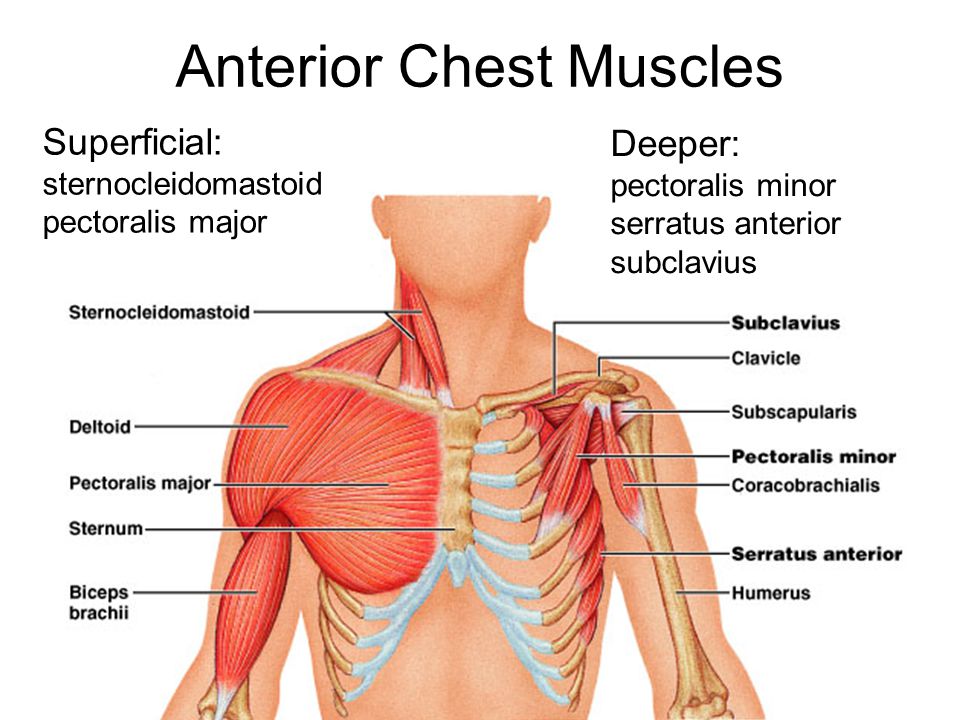 J Natl Cancer Inst 1996;88
J Natl Cancer Inst 1996;88
(13)
890- 899PubMedGoogle ScholarCrossref
10.
Forastiere
А.А.Гёпферт
Хмаор
М
и другие. Сопутствующая химиотерапия и лучевая терапия для сохранения органов при распространенном раке гортани. N Engl J Med 2003;349
(22)
2091- 2098PubMedGoogle ScholarCrossref
11.
Ханна
EY Сохранение гортани: какова наилучшая стратегия лечения? Curr Oncol Rep 2004;6
(3)
167- 169PubMedGoogle ScholarCrossref
12.
Лефевр
JL Сохранение гортани при раке головы и шеи: мультидисциплинарный подход. Ланцет Онкол 2006;7
(9)
747- 755PubMedGoogle ScholarCrossref
13.
Пайдарфар
Я.Биркмейер
Нью-Джерси Осложнения в хирургии головы и шеи: метаанализ кожно-глоточных свищей после ларингэктомии. Arch Otolaryngol Head Neck Surg 2006;132
(1)
67- 72PubMedGoogle ScholarCrossref
14.
Вебер
RSBerkey
BAForastiere
А
и другие. Исход спасительной тотальной ларингэктомии после органосохраняющей терапии: исследование Radiation Therapy Oncology Group 91-11. Arch Otolaryngol Head Neck Surg 2003;129
(1)
44- 49PubMedGoogle ScholarCrossref
15.
Смит
Т. Дж. Беррадж
К.Дж.Гангули
ПКирби
СДровер
C Профилактика кожно-глоточных свищей после ларингэктомии: опыт Мемориального университета. J Отоларингол 2003;32
(4)
222- 225PubMedGoogle ScholarCrossref
16.
Ригини
Клеке
ТКюинье
Оморел
НРейт
E Грудной миофасциальный лоскут в фаринголарингеальной хирургии после лучевой терапии. Eur Arch Otorhinolaryngol 2005;262
(5)
357- 361PubMedGoogle ScholarCrossref
17.
Albirmawy
ОА Профилактика постларингэктомического кожно-глоточного свища с использованием лоскута воротника грудино-ключично-сосцевидной мышцы. Дж Ларынгол Отол 2007;121
(3)
253- 257PubMedGoogle ScholarCrossref
18.
Fung
КТекнос
Т.Н.Ванденберг
компакт диск
и другие. Профилактика раневых осложнений после спасительной ларингэктомии с использованием свободной васкуляризированной ткани. Шея головы 2007;29
(5)
425- 430PubMedGoogle ScholarCrossref
19.
Сингх
BBhaya
MStern
Дж
и другие. Валидация индекса коморбидности Чарлсона у пациентов с раком головы и шеи: многоцентровое исследование. Ларингоскоп 1997;107
(11, ч. 1)
1469- 1475PubMedGoogle ScholarCrossref
20.
Шах
JPGil
Z Текущие концепции лечения рака полости рта — хирургия. Онкол для полости рта 2009;45
(4-5)
394- 401PubMedGoogle ScholarCrossref
21.
Ньюман
JPTerris
DJPinto
HAFee
МЫ
младший Гуд
РЛГоффинет
DR Хирургическая заболеваемость расслоением шеи после химиолучевой терапии при распространенном раке головы и шеи. Энн Отол Ринол Ларингол 1997;106
(2)
117- 122PubMedGoogle Scholar
22.
Пьяцца
CPeretti
GCattaneo
АГаррубба
ФДе Зинис
LOНиколай
P Спасительная хирургия после лучевой терапии рака гортани: от эндоскопических резекций до частичной и тотальной ларингэктомии с открытой шеей. Arch Otolaryngol Head Neck Surg 2007;133
(10)
1037- 1043PubMedGoogle ScholarCrossref
23.
Парих
SRирландский
Дж.Курран
Эй Джей Гуллан
ПиДжейБраун
Д. Х. Ротштейн
LE Кожно-глоточные свищи у пациентов с ларингэктомией: опыт больницы Торонто. J Отоларингол 1998;27
(3)
136- 140PubMedGoogle Scholar
24.
Грау
Си Йохансен
Л.В.Хансен
ГС
и другие. Спасительная ларингэктомия и кожно-глоточные свищи после первичной лучевой терапии рака головы и шеи: национальное исследование DAHANCA. Головка Шея 2003;25
Головка Шея 2003;25
(9)
711- 716PubMedGoogle ScholarCrossref
25.
Виртаниеми
Я.Кумпулайнен
Э. Дж. Хирвикоски
П.П.Йоханссон
РТКосма
В. М. Частота возникновения и этиология кожно-глоточных свищей после ларингэктомии. Шея головы 2001;23
(1)
29- 33PubMedGoogle ScholarCrossref
26.
Вайнград
DNSpiro
RH Осложнения после ларингэктомии. Am J Surg 1983;146
(4)
517- 520PubMedGoogle ScholarCrossref
Chest Opening Exercises to Wake Up Your Pectoralis Minor
Subscribe
CategoriesAnatomyAudioBack PainBalanceBeginnersBreathingCalvesCancerCoreCyclingDancersDigestionEvents & TrainingsFace and JawFasciaFeet & AnklesFlexibility & StretchingForearmsGolfHands & WristsHeadaches & MigrainesHipsHips & GlutesInjuries & AccidentsInternal OrgansInterviewJill MillerKneesLegsMassage ToolsMeet the TeacherMindsetMobilityNeck & HeadPain SciencePelvic FloorPostnatalPosturePregnancyRecovery & AddictionRunningSciatic PainSelf -MassageShouldersSleepSpineСила и кондиционированиеСтресс и напряжениеХирургияТехники обученияКомандные виды спортаТеннисТравмы и посттравматическое стрессовое расстройствоБез рубрикиВидеоУправление весомЖенское здоровье
AuthorsAda-Reva SpaeAlex IgleciaAlexa KimAlexandra EllisAlexandra LariviereAli BellAlison PignoletAllison McCreadyAmalea FisherAmanda CrutcherAmanda JoyceAmanda MorleyAmanda TrippAmanda WinklerAmanda ZerbiniAmy DeguioAnnelie AlexanderAnnMerle FeldmanAriana RabinovitchAriel KileyBaylea MicheliBeth DammBo OConnorBonnie GoldenBrooke ThomasCaitlin VestalCari Devine BjelajacCathy FavelleChadd SchaeferChristina BroomeChristina MedinaChristina SummervilleChristine JablonskiClaiborne DavisClaire MillerCorey WrightDagmar KhanDawn AdamsDawn MauricioDawn McCroryDiane MarraDinneen ViggianoElaine JacksonElise FabricantElissa StruttonElizabeth WipffEmilie MikullaEmily PantaloneErin KintzingGenevieve HerzogGiancarla Griffith-BoyleGwen YeagerHeather LongoriaHeidi BroeckingHolli RabishawIlene CohenJamie LeighJasmine EllemoJason CampbellJeff LaneJeffrey LangJenni RawlingsJennie CohenJennifer LovelyJennifer WendeJessie DwigginsJill MillerJohn GreenhowJonathan McKinnaKate Duyn CariatiKate Hamm Kate KrumsiekKathy HotchkissKatie RuttererKayleigh MillerKeith WittensteinKendra ZanottoKevyn McAnlisKirsten TruedKristen ButeraKristin GardnerKristin MarvinKyoko JasperLana GoldbergLara WeithornLaurel BeversdorfLauren CapLaurie StreffLee-Anne HeronLeslie WrightLillee ChandraLindsay ClearyLindsay SmithLinh TaylorLisa FedericoLisa HebertLisa SansonLiz RobertsLouis JacksonLuke SniewskiLynda JaworskiMacala ShonMacklen MayseMandy PansingMaria VogelMarla BrackmanMatt SharpeMatthew CoeMax BayukMaya TalisaMelinda KausekMeredith AmannMeredith Hutter ChamorroMichelle PitmanMiriam RigneyMissy MoriartyMonica BrightNajla SaidNancy BellantoniNancy CochrenNicole QuibodeauxNicole RadziszewskiNicolette DavidNikki WongPamela FernerPamela ForthPatty WorthamRachel TaylorRebecca TammRenee DelloRhonda BraunRiannon ZornRobyn CapobiancoSamara AndradeSandy ByrneSandy GrossSara KaySara WolversonSarah CourtShakti RowanShari WilliamsShelley PiserSherry MatweSierra AleaSiewli StarkStephanie LegerSue McGurnSue Tay лорСюзанна КровиакТамара КоулТэмми ГруберТерри ЛиттлфилдТесс БоллТиа УкпеТиффани Чемберс-ГолдбергТиффани ХолмсТодд ЛавиктуарТрина АльтманTune Up Fitness TeamVia PageЯсмен МехтаЮМи ЧангИвонн Коун
Подписаться
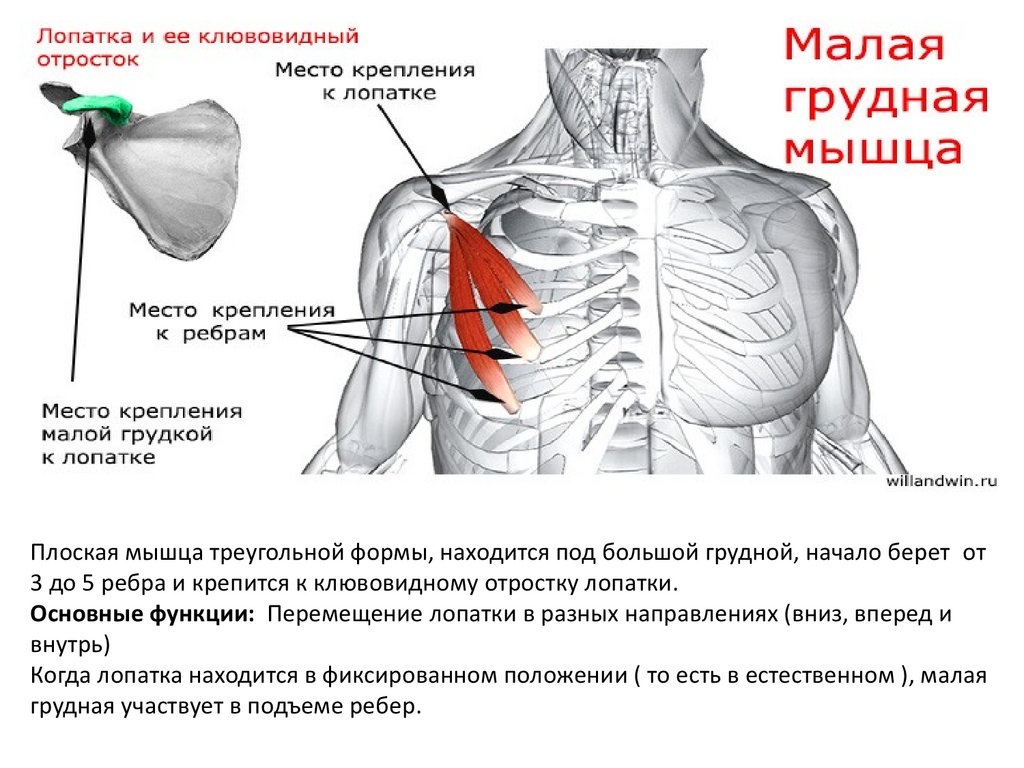
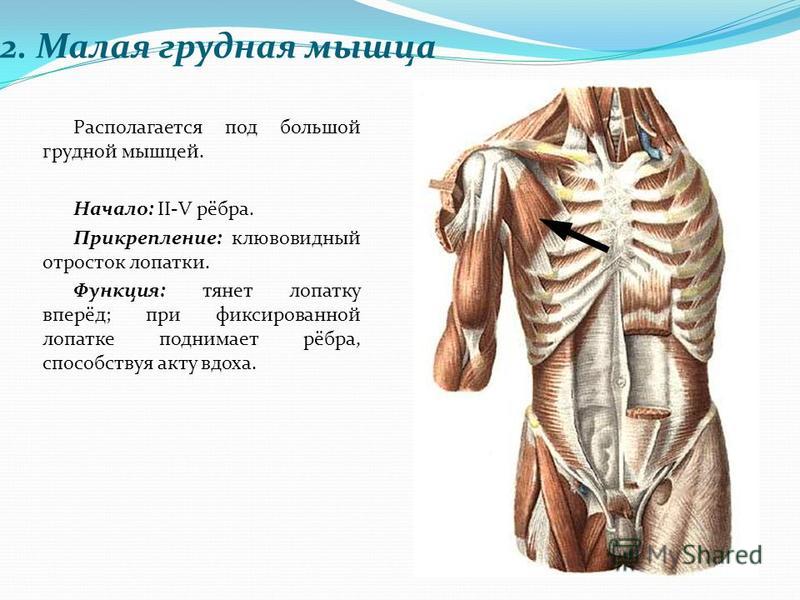
Одна вещь, на которой я всегда сосредотачиваюсь на своих занятиях, это раскрытие грудной клетки, чтобы создать пространство для большего дыхания, и хотя мы, йоги, всегда думаем о прогибах назад и сокращении мышц спины для раскрытия грудной клетки, иногда нам нужно обратить внимание на мышцы на передний корпус. Например, малая грудная мышца скрыта под большой грудной мышцей; несмотря на свой размер, это жизненно важная мышца для здоровья плеча в частности и общего состояния здоровья в целом. Малая грудная мышца начинается от третьего, четвертого и пятого ребер и прикрепляется к клювовидному отростку лопатки; таким образом, эта маленькая мышца соединяет лопатку с грудной клеткой. Его основная функция — помогать приподнимать грудную клетку во время вдоха, обеспечивая полное и глубокое дыхание. То есть в идеальном мире.
Например, малая грудная мышца скрыта под большой грудной мышцей; несмотря на свой размер, это жизненно важная мышца для здоровья плеча в частности и общего состояния здоровья в целом. Малая грудная мышца начинается от третьего, четвертого и пятого ребер и прикрепляется к клювовидному отростку лопатки; таким образом, эта маленькая мышца соединяет лопатку с грудной клеткой. Его основная функция — помогать приподнимать грудную клетку во время вдоха, обеспечивая полное и глубокое дыхание. То есть в идеальном мире.
Большинство из нас, из-за нашего распорядка дня, не имеют полного диапазона движений в малой грудной мышце. Мы проводим так много времени, сгорбившись, с повернутыми внутрь плечами и выдвинутыми лопатками — перед компьютерами, над рулем, опираясь на прилавок, когда нарезаем овощи и другие продукты для еды, сгорбившись над цветочными клумбами во время работы в саду и так далее. — что эта мышца хронически укорачивается, вытягивая лопатки вперед и ставя под угрозу способность грудной клетки расширяться. Кроме того, когда эта мышца сжимается, основные кровеносные сосуды руки, а также плечевое сплетение (нервы, иннервирующие руку), которые проходят под ней, также сдавливаются, и их функция нарушается, вызывая онемение и нарушение кровообращения. Нам нужно изменить эту привычную позу для нашего дыхания, здоровья наших плеч (диапазон движений и гибкость) и нашего общего здоровья (например, возможность дотянуться до шкафа над головой и почесать себе спину сзади).
Кроме того, когда эта мышца сжимается, основные кровеносные сосуды руки, а также плечевое сплетение (нервы, иннервирующие руку), которые проходят под ней, также сдавливаются, и их функция нарушается, вызывая онемение и нарушение кровообращения. Нам нужно изменить эту привычную позу для нашего дыхания, здоровья наших плеч (диапазон движений и гибкость) и нашего общего здоровья (например, возможность дотянуться до шкафа над головой и почесать себе спину сзади).
Хорошей новостью является то, что «повреждение» можно легко исправить с помощью упражнений с мячом и нескольких растяжек, которые занимают очень мало времени. Поскольку большую часть рабочего дня я провожу за компьютером, у меня появилось особое пристрастие к регидратации и мобилизации малой грудной мышцы. Моя любимая последовательность заключается в том, чтобы взять терапевтический мяч YTU и блок к стене, поместить мяч на блок, а затем перекатывать из-под внутренней ключицы к внешней ключице, осторожно нажимая на клювовидный отросток (шишковидный выступ на плече). лезвие, которое торчит в область подмышек), когда я до него доберусь. Это движение также разворачивает подключичную кость, которая поднимает первое ребро во время вдоха — бонус! Затем я перехожу к варианту чистки плечевой нити № 1 (используя ремень, чтобы перемещать плечевой пояс вперед и назад посредством кругового движения) в течение четырех или пяти подходов (больше, если у меня есть время). На этом можно было бы остановиться и ощутить преимущества, но если есть больше времени, я хотел бы добавить в Прасариту «Мост руки» и «Сезам, откройся». Попробуйте эти упражнения на раскрытие грудной клетки — ваше дыхание уже не будет прежним.
лезвие, которое торчит в область подмышек), когда я до него доберусь. Это движение также разворачивает подключичную кость, которая поднимает первое ребро во время вдоха — бонус! Затем я перехожу к варианту чистки плечевой нити № 1 (используя ремень, чтобы перемещать плечевой пояс вперед и назад посредством кругового движения) в течение четырех или пяти подходов (больше, если у меня есть время). На этом можно было бы остановиться и ощутить преимущества, но если есть больше времени, я хотел бы добавить в Прасариту «Мост руки» и «Сезам, откройся». Попробуйте эти упражнения на раскрытие грудной клетки — ваше дыхание уже не будет прежним.
Узнайте больше о своей диафрагме.
Узнайте о наших продуктах для снятия стресса.
Узнайте о наших программах Therapy Ball.
Прочитайте, как избавиться от стресса.
Доун Адамс
Дон занимается йогой с середины 1990-х годов. Она взяла свой первый урок на станции йоги Аламеда в 1996 году и с тех пор училась у опытных учителей, таких как Сэнди Блейн, Джоанн Лайонс и Дональд Мойер.